Training voor QC Leiden People Leaders
Driving Results through Individual & Organizational Accountability


Proud to be Leiden QC
Ensuring quality, supporting
the world
Ondertitel?
Batch Release made easy!
Ik ben heel blij dat de Batch RelEASY-applicatie in oktober vorig jaar met succes is gelanceerd. Deze innovatie verbetert de operationele efficiëntie en zorgt ervoor dat de Quality Standards worden nageleefd. Batch RelEASY is een van de eerste applicaties die GxP-rapporten live genereert op het Self-Service Statistical Reporting Platform.
Wat is Batch RelEASY?
Batch RelEASY is een digitale tool voor het maken van rapporten die het genereren van release packages automatiseert en eenvoudiger maakt voor Remicade, Stelara en Simponi (P)FB materiaal op onze Bio sites in Leiden en Cork. Het haalt data op uit onze bronsystemen, zoals SAP, MES, eLIMS, Trackwise en binnenkort Comet, en organiseert deze in rapporten die nodig zijn voor batch release. Het is echter geen transactiesysteem voor batch release. Het registreert geen beslissingen, activiteiten of data. De gegenereerde rapporten vragen om een 'handmatige review stap' op volledigheid, door een QA Officer, voordat een QP ze beoordeelt voor batch release.
De reis – Succes is niet altijd direct een feit, en onze reis was daarop geen uitzondering. In eerste instantie probeerden we Tableau te gebruiken om releaserapporten te genereren, maar dat bleek niet haalbaar. Dit leidde ertoe dat we andere opties onderzochten en uiteindelijk Posit.co kozen als het platform van onze keuze. Posit biedt een betere manier om op R & python gebaseerde oplossingen te implementeren en stelt developers in staat om de open-source tools te gebruiken die ze kennen en waar ze van houden, met het gecentraliseerde beheer, de beveiliging en de ondersteuning die ze nodig hebben.
“De moeite vermindert van uren tot slechts een minuut”
In december 2022 kregen we groen licht van de wereldwijde Digital & Technology Council om Posit voor Batch RelEASY-ontwikkeling aan boord te nemen en te implementeren. Budgetgoedkeuring volgde in april 2023 en we begonnen met de bouw van Batch RelEASY. Het platform werd binnen J&J omgedoopt tot het Self-Service Statistical Reporting Platform (SSSR) en in januari 2024 werd het opgeleverd als een volledig GxP-compliant applicatie. In de zomerperiode hebben we de gebruikersacceptatietests voor Batch RelEASY uitgevoerd en de kwalificatie afgerond. Als eerste gebruiker van dit nieuwe platform werden we geconfronteerd met tal van uitdagingen.
Door gebruik te maken van agile methodologie en het software development life cycle (SDLC) framework werd Batch RelEASY op 29 oktober succesvol gelanceerd op de Bio sites in Leiden en Cork.
Noor Vroege-Tielen is Senior Manager of the AVA and Mycoplasma team within Quality Control at Johnson & Johnson Innovative Medicine, Biologics in Leiden. In this blog, she shares what makes her proud to be part of the Leiden QC team, and how their work helps ensure the safety and quality of medicines for patients around the world.
When I first joined Johnson & Johnson Innovative Medicine, Biologics in Leiden, my manager Harold Backus told me, “We’re proud to be Leiden Quality Control.” It was more than just a motto – it reflected genuine passion, ownership, and pride in the work being done here. Now, almost a year later, I can wholeheartedly say: I feel the same.
As Senior Manager of the Adventitious Virus Assay (AVA) and Mycoplasma team within Quality Control (QC), I work alongside a dedicated group of scientists, specialists and supervisors who bring incredible expertise, precision, and passion to their work. What energizes me most is working in a team where scientific knowledge meets real-world impact – where every test we run plays a role in ensuring patient safety around the globe.
A global QC hub
The scope and importance of QC Biotherapeutics in Leiden are impressive: our team of 300 colleagues plays a unique and essential role in the global J&J network. We are not only testing locally manufactured products – 75% of the samples we analyze come from manufacturing sites around the world. That means our work touches nearly every biologic product that J&J produces globally.
“The future of QC in Leiden is filled with opportunities”
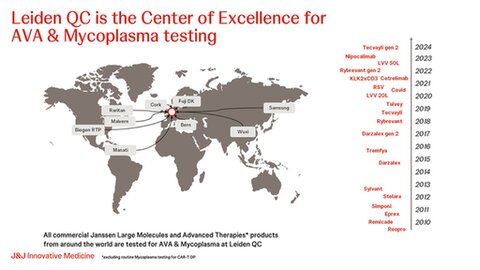
We serve as a quality control hub for the company, particularly when it comes to stability testing, raw material release, and AVA and Mycoplasma testing. Our laboratory in Leiden is the only site in the entire J&J network that performs AVA and Mycoplasma testing. These assays are critical for ensuring the absence of unwanted viruses and mycoplasma contamination in our Biotherapeutic and Advance Therapies products, which could impact both product safety and manufacturing efficiency.
As the Stability Hub of the global network, we manage long-term stability studies for various batches, combining them where possible to increase testing efficiency and optimize operational costs across the supply chain. This doesn’t just benefit the company – it helps ensure timely access to safe, effective medicines for patients.

Microbial analysis at QC
Excellence in action
QC is woven into the fabric of J&J’s broader mission. We’re not just a support function – we are one of the four strategic pillars of J&J IM Biologics in Leiden. QC’s strategic importance is shown through ongoing investments from the organization: from building state-of-the-art labs and setting up rapid testing methods, to implementing “My Green Lab” certification and driving continuous improvement through A3s and FPX. QC is clearly seen, heard, and empowered to lead. This enables us to take true ownership of our direction – identifying opportunities, setting priorities, and delivering lasting impact across the network.
Looking ahead
The future of QC in Leiden is filled with opportunities. As the product portfolio grows, so will the diversity and complexity of our testing. We’re ready to meet these challenges with agility and innovation. Our commitment to digitalization, AI integration, Lean Lab approaches, and sustainability is already transforming how we work. What keeps me going is knowing that every test we run contributes to a bigger mission: ensuring the safety and efficacy of the medicines patients depend on. Without QC, production halts. Without QC, medicines can’t be released. Without QC, patients don’t get what they need.
So yes – I’m proud to be Leiden QC. It’s more than a phrase. It’s who we are.

Noor Vroege-Tielen
Sr. Manager AVA/MYCO at QC
Ondertitel
Ondertitel

Ondertitel
Ondertitel

Ondertitel